
- Outeur Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:12.
- Laas verander 2025-01-22 15:50.
Definisie. Die farmaseutiese Kwaliteit volgens ontwerp (QbD) is 'n sistematiese benadering tot ontwikkeling wat begin met voorafbepaalde doelwitte en beklemtoon produk- en prosesbegrip en prosesbeheer, gebaseer op grondige wetenskap en kwaliteit risiko bestuur.
Waarom is kwaliteit volgens ontwerp ook nodig?
Kwaliteit deur Ontwerp is 'n strategiese, sistematiese benadering om jou nuwe produkpyplyn vinniger, makliker, vir minder te bemark. Kwaliteit volgens ontwerp klem op gesonde wetenskap, logiese beheermaatreëls en risikobestuur bespoedig konsekwent tyd tot mark, verminder koste en verhoog sukses.
U kan ook vra: wat is RLD in QbD? Die RLD is 'n onmiddellike vrystelling (IR) tablet wat aangedui word vir die verligting van matige tot ernstige fisiologiese simptome. Ons het Quality by Design gebruik ( QbD ) om generiese asetriptan IR-tablette te ontwikkel wat terapeuties gelykstaande is aan die RLD.
Net so, wat is kwaliteit ontwerp TQM?
Kwaliteit van ontwerp word gedefinieer as 'n passing tussen 'n produk (diens s'n) ontwerp en behoeftes van die kliënt; kwaliteit ooreenstemming word gedefinieer as 'n pasvorm tussen die eienskappe van 'n werklike produk en die spesifikasie daarvan. Om kliënte tevrede te stel, kwaliteit moet hoog op beide afmetings wees.
Wat is ontwerpruimte in QbD?
Ontwerpruimte in QbD - Definisies. Vir die wetenskaplike, Ontwerp ruimte is 'n Y(Kwaliteitskenmerke) = F (Prosesparameters, Materiaalkenmerke) - 'n funksie of 'n verwantskap tussen (kritiese) prosesparameters en (kritiese) kwaliteitseienskappe /materiaalkenmerke.
Aanbeveel:
Wat is FDA CFR 21?

Titel 21 is die deel van die Code of Federal Regulations wat voedsel en dwelms in die Verenigde State beheer vir die Food and Drug Administration (FDA), die Drug Enforcement Administration (DEA) en die Office of National Drug Control Policy (ONDCP)
Wat kan ek verwag van 'n FDA-inspeksie?

Wat om te verwag by die fasiliteit tydens 'n FDA inspeksie Toerusting kalibrasie en instandhouding verslae. Interne ondersoeke na die hoofoorsake van produksiemislukkings. Verwerk valideringsverslae. Produksie- en prosesbeheerverslae. Afwykings verslae. Interne ouditverslae. Statistiese evaluering van produkdata
Hoe definieer die American Society for Quality kwaliteit?

Die American Society for Quality (ASQ) definieer kwaliteit as 'die geheel van kenmerke en kenmerke van 'n produk of diens wat verband hou met sy vermoë om gegewe behoeftes te bevredig'
Wat is CFR in FDA?

Die Kode van Federale Regulasies (CFR) is 'n kodifikasie van die algemene en permanente reëls gepubliseer in die Federale Register deur die Uitvoerende departemente en agentskappe van die Federale Regering.. Titel 21 van die CFR is gereserveer vir reëls van die Food and Drug Administration
Hoe gebruik jy Total Quality Management?
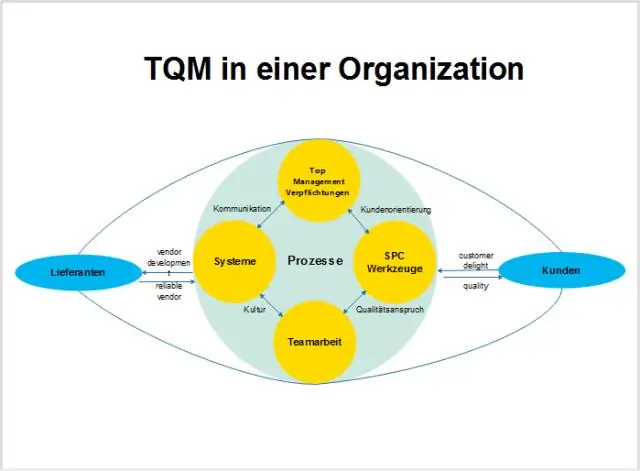
Stappe om 'n totale kwaliteitbestuurstelsel te skep Verhelder visie, missie en waardes. Identifiseer kritiese suksesfaktore (CSF) Ontwikkel maatstawwe en statistieke om CSF-data op te spoor. Identifiseer sleutelkliëntegroep. Vra terugvoer van kliënte. Ontwikkel 'n opname-instrument. Ondersoek elke klantegroep. Ontwikkel verbeteringsplan
