
INHOUDSOPGAWE:
- Outeur Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:12.
- Laas verander 2025-06-01 04:48.
A 510 (k ) is 'n voorlegging wat inligting bevat wat vereis word onder 21 CFR 807.87. Vir meer inligting oor die regulatoriese raamwerk, beleide en praktyke onderliggend aan die FDA se 510(k ) resensie, verwys asseblief na die leiding Die 510 (k ) Program: Evaluering van wesenlike ekwivalensie in voormarkkennisgewing [ 510 (k )].
Behalwe dit, wat is 'n 510k liassering?
A 510 (K ) is 'n voormark voorlegging gemaak om FDA om te demonstreer dat die toestel wat bemark moet word ten minste net so veilig en doeltreffend is, dit wil sê, wesenlik gelykstaande aan 'n wettig bemarkde toestel (21 CFR §807.92(a)(3)) wat nie onderhewig is aan voorafmarkgoedkeuring nie. Kom meer te wete Soek databasis. Help om lêers af te laai. 510K
Net so, wat is 'n spesiale 510k? Spesiale 510(k )s laat die FDA en industrie om staat te maak op vorige agentskap se hersiening van gedetailleerde inligting, waar toepaslik, sonder om enige statutêre of regulatoriese vereistes te verander wat verband hou met die voormarkkennisgewingproses kragtens artikels 510 en 513 van die FD&C Wet, en 21 CFR 807 Subdeel E.
Hoe berei jy 'n 510 K daarvan voor?
Om mee te begin, hier is 'n lys van al die afdelings wat benodig word vir 'n 510(k) indiening:
- Groep 1 - Voorbladvorms.
- Groep 2 - Wat ander kan sien.
- Groep 3 - Sjabloonafdelings.
- Groep 4 - Vergelyk jou produk vs. predikaat(e)
- Groep 5 - Versekering van pasiëntveiligheid.
- Groep 6 - Sagteware en Elektronika.
- Groep 7 - Prestasietoetsing.
Wat is die verskil tussen 510k en PMA?
A PMA is meer in-diepte as a 510k - dit word gebruik om te bewys dat 'n nuwe toestel veilig en effektief is vir die eindgebruiker en vereis tipies kliniese proewe met menslike deelnemers saam met laboratoriumtoetse.
Aanbeveel:
Wat is 'n probleem wat verband hou met afloop van kunsmis?

Omgewingsimplikasies van oormaat kunsmis en mis op waterkwaliteit (NM1281, hersien Oktober
Wat is die siklus wat die huismark volg?
Die vier elementêre fases van die behuisings- of werklike staatsmark is die herstelfase, die uitbreiding, die hiperaanbod en resessie. Net soos enige ander mark wat van baie faktore afhang, het die huismark sy ups en downs. 'N Belangrike oorweging is dat die fases op verskillende markte kan verskil
Wat is 'n alternatief vir kunsmis wat op stikstof gebaseer is?
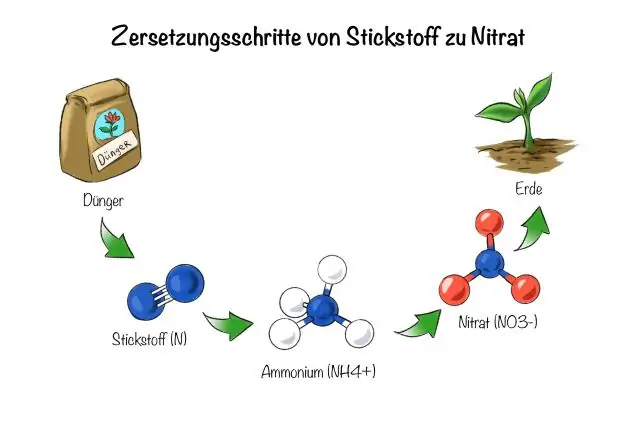
Daar is verskillende alternatiewe vir chemiese bemesting by die meeste tuinsentrums en kweekhuise wat natuurlike materiale gebruik om u grond te verryk. Beenmaal. Katoensaadmeel. Lusernkorrels. Vlermuis Guano. Vis emulsies. Gekomposteerde mis
Wat is die belangrikste magte wat aan die Kongres gegee word?

Dit sluit in die mag om oorlog te verklaar, geld te munt, 'n weermag en vloot op te rig, handel te reguleer, reëls vir immigrasie en naturalisasie op te stel, en die federale howe en hul jurisdiksies daar te stel
Wat is die naam wat algemeen gegee word aan die vloeistof wat gebruik word om 'n put te boor?

Emulsies: Die twee tipes wat gebruik word is olie in water (olie-emulsie modder) en water in olie (omgekeerde olie emulsie modder)
